سندروم آلپورت به نامهای مختلفی شناخته میشود:
اسامی مشترک سندرم آلپورت:
ناشنوایی هماتوریا-نفروپاتی (سابق) “hematuria-nephropathy deafness”
نفریت خانوادگی خونریزی دهنده (سابق) “hemorrhagic familial nephritis”
ناشنوایی و نفروپاتی ارثی (سابق) “hereditary deafness and nephropathy”
نفریت ارثی (سابق) “hereditary nephritis”
نفریت ارثی با ناشنوایی حسی (سابق) “hereditary nephritis with sensory deafness”
زیرمجموعههای سندرم آلپورت کدامند؟
سندرم آلپورت اتوزومال غالب (ADAS) “autosomal dominant Alport syndrome”
سندرم آلپورت اتوزوم مغلوب (ARAS) “autosomal recessive Alport syndrome”
سندرم آلپورت مرتبط با X (XLAS) “X-linked Alport syndrome”
فهرست مطالب
در مورد سندروم آلپورت بیشتر بدانیم
سندرم آلپورت یک اختلال ژنتیکی نادر است که با بیماری پیشرونده کلیه و ناهنجاریهای گوش داخلی و چشم مشخص میشود. سه نوع ژنتیکی از این سندرم وجود دارد. سندرم آلپورت مرتبط با X (XLAS) شایعترین نوع این اختلال است. به طور معمول مردان مبتلا در انواع این اختلال، به بیماری شدیدتری نسبت به زنان دچار میشوند. در سندرم آلپورت اتوزومال “autosomal” مغلوب (ARAS) شدت بیماری در مردان و زنان مبتلا مشابه است. یک نوع از اختلال اتوزومال غالب (ADAS) نیز وجود دارد که مردان و زنان را با شدت برابر تحت تأثیر قرار میدهد. مشخصه اصلی بیماری وجود خون در ادرار (هماچوری “hematuria”) در اوایل زندگی، همراه با کاهش تدریجی عملکرد کلیه (نارسایی کلیه) است که در نهایت منجر به نارسایی کلیه به ویژه در مردان مبتلا میشود. حدود 50٪ از مردان درمان نشده با XLAS تا 25 سالگی دچار نارسایی کلیه میشوند؛ این درصد در 40 سالگی به 90٪ و در 60 سالگی به 100٪ افزایش مییابد. به طور معمول زنان مبتلا به XLAS تا اواخر زندگی دچار نارسایی کلیه نمیشوند. این احتمال وجود دارد که به هیچ وجه دچار عوارض بیماری یا نارسایی کلیه نشوند اما با افزایش سن خطر بروز این شرایط افزایش مییابد. اغلب مردان و زنان مبتلا به ARAS در سن بلوغ یا اوایل بزرگسالی دچار نارسایی کلیه میشوند.
اختلال ADAS تمایل دارد که یک بیماری کند با پیشروی آرام باشد که در آن نارسایی کلیه تا زمان بزرگسالی ایجاد نمیشود. همچنین افراد مبتلا به سندرم آلپورت ممکن است دچار کاهش شنوایی پیشرونده با شدت و ناهنجاریهای مختلف چشم شوند که این وضعیت به طور معمول منجر به اختلال در بینایی نمیشود. XLAS توسط انواع مختلف ژن COL4A5 ایجاد میشود. ARAS توسط انواع مختلف در هر دو نسخه از ژن COL4A3 یا COL4A4 ایجاد میگردد. ADAS توسط انواع موجود در یک نسخه از ژن COL4A3 یا COL4A4 ایجاد میشود. سندرم آلپورت به صورت علامتی درمان میشود و برخی از داروها میتوانند به طور بالقوه پیشرفت بیماری کلیه و شروع نارسایی کلیه را به تأخیر بیندازند. در نهایت در بسیاری از بیماران، پیوند کلیه مورد نیاز است.
معرفی کامل سندرم آلپرت
بیماری که اکنون به عنوان سندرم آلپورت میشناسیم اولین بار در سالهای اولیه قرن 20 در ادبیات پزشکی انگلیس توصیف شد. در سال 1927 دکتر سیسیل آلپورت مقالهای را منتشر کرد که در آن ارتباط بیماری کلیوی و ناشنوایی در افراد مبتلا شرح داده شد. بسیاری از موارد اضافی در کتاب پزشکی شرح داده شد و این اختلال به نام دکتر آلپورت در سال 1961 نامگذاری شد. اغلب سندرم آلپورت با یک اختلال مرتبط شناخته شده به عنوان نفروپاتی غشای پایه نازک (TBMN) که در آن ناهنجاری غالب پاتولوژیک نازک شدن گلومرول “glomerular” وجود دارد، مشاهده میشود. بسیاری از افراد مبتلا به TBMN دارای انواع مختلفی از غشاها در ژنهای مشابه هستند که این شرایط باعث بروز سندرم آلپورت میشود. افراد مبتلا به TBMN به شکل مشابهی دارای خون میکروسکوپی مداوم در ادرار (هماچوری) هستند که در افراد مبتلا به سندرم آلپورت مشاهده میشود. در بیمارانی که تشخیص TBMN داده شده است کمتر از بیماران مبتلا به سندرم آلپورت علائم خارج از کلیه (ناهنجاریهای خارج از کلیه) وجود دارد؛ عوارض و اختلالات اضافی کلیه مانند پروتئین در ادرار (پروتئینوریا “proteinuria”)، فشار خون بالا (hypertension)، نارسایی کلیه، و ناهنجاریهای کلیه از سندرم آلپورت کمتر است. در بیمارانی که هماچوری و انواع مختلفی از ژنهای COL4A3 ، COL4A4 یا COL4A5 دارند، میبایست سندرم آلپورت تشخیص داده شود در حالی که مبتلایان به غشای پایه گلومرولی نازک که هیچ گونه تغییری در این ژنها ندارد، باید با هماچوری غشای زیرین گلومرولی نازک تشخیص داده شوند. افتراق سندرم آلپورت و TBMN خصوصاً در بیماران جوان و در خانمها میتواند چالش برانگیز باشد. به منظور کسب اطلاعات بیشتر در مورد این موضوع مقاله را مطالعه نمایید.

علائم و نشانههای سندرم آلپورت کدامند؟
شروع، علائم، پیشرفت و شدت سندرم آلپورت میتواند از یک فرد به فرد دیگر بسیار متفاوت باشد؛ این موضوع تا حدی به نوع خاص و نوع ژن موجود بستگی دارد. برخی از افراد ممکن است نوعی اختلال خفیف و آهسته پیشرونده داشته باشند، در حالی که در برخی دیگر عوارض شدید وجود دارد.
اولین نشانهها
اولین نشانه بیماری کلیه، وجود خون در ادرار (هماچوری) است. به طور معمول هماچوری با چشم غیر مسلح قابل مشاهده نیست اما وقتی ادرار تحت میکروسکوپ بررسی میشود، قابل مشاهده است. این وضعیت را هماچوری میکروسکوپی میگویند. گاهی اوقات این احتمال وجود دارد که خون برای مدت چند روز در ادرار قابل مشاهده باشد (به عنوان مثال ادرار ممکن است قهوهای، صورتی یا قرمز باشد)؛ به طور معمول این شرایط زمانی اتفاق میافتد که فرد مبتلا به سرماخوردگی یا آنفولانزا باشد. این شرایط به عنوان نوعی از هماچوری فاحش شناخته میشود. به طور معمول مردان مبتلا به XLAS در اوایل زندگی خود، هماچوری میکروسکوپی مداوم را بروز میدهند. حدود 95٪ از زنان مبتلا به سندرم XLAS دارای هماچوری میکروسکوپی هستند اما این اختلال ممکن است بیاید و برود (به طور متناوب تغییر کند). مردان و زنان مبتلا به ARAS در دوران کودکی به هماچوری مبتلا میشوند. همچنین مردان و زنان مبتلا به ADAS، هماچوری دارند.
در گذر زمان علائم چگونه خواهند شد؟
با گذشت زمان بسیاری از افراد مبتلا به این اختلال، سطح بالایی از آلبومین “albumin” و سایر پروتئینها را در ادرار خود نشان میدهند (آلبومینوریا و پروتئینوریا “albuminuria and proteinuria”) که نشانههایی از پیشرفت بیماری کلیه است. مرحله بعدی پیشرفت، کاهش تدریجی عملکرد کلیه است که غالباً با فشار خون بالا (hypertension) همراه است تا این که در نهایت کلیهها از کار میافتند (مرحله انتهایی بیماری کلیوی یا ESRD). کلیهها عملکردهای مختلفی از جمله فیلتر کردن و دفع مواد زائد از خون و بدن، ایجاد هورمونهای خاص و کمک به حفظ تعادل برخی مواد معدنی در بدن مانند پتاسیم، سدیم، کلرید و سایر الکترولیتها دارند. علائم مختلفی میتواند با ERSD همراه باشد از جمله ضعف و خستگی، تغییر در اشتها، پف یا تورم (ورم)، ضعف هضم غذا، تشنگی بیش از حد و تکرر ادرار.
همان طور که در بالا ذکر شد، میزان پیشرفت بیماری کلیه بسیار متفاوت است. بسیاری از پسران مبتلا به XLAS تا سن بلوغ یا اوایل بزرگسالی دچار ERSD میشوند، اگرچه برخی از آنها تا 40 یا 50 سالگی دچار نارسایی کلیه نخواهند شد. بیشتر زنان مبتلا به XLAS تا اواخر زندگی دچار نارسایی کلیه نمیشوند. نارسایی کلیه تعداد کمتری از مردان مبتلا به XLAS را درگیر میکند اما هنوز هم خطر قابل توجهی دارد، در حدود 15٪ در سن 45 سالگی و 20-30٪ در سن 60 سالگی.
کاهش شنوایی پیشرونده (ناشنوایی حسی عصبی) به طور مکرر در افراد مبتلا به سندرم آلپورت رخ میدهد. ناشنوایی حسی-عصبی ناشی از اختلال در انتقال صدا از گوش داخلی (حلزون گوش) به مغز از طریق اعصاب شنوایی است. کاهش شنوایی دو طرفه است، یعنی هر دو گوش را تحت تأثیر قرار میدهد. به طور معمول کاهش شنوایی در اواخر کودکی در پسران مبتلا به XLAS مشهود است، اگرچه ممکن است خفیف یا ضعیفشده باشد. در مردان مبتلا به XLAS، فراوانی کمشنوایی در سن 15 سالگی تقریباً 50٪، در 20 سالگی 75٪ و در 40 سالگی 90٪ است. کاهش شنوایی، پیشرونده است و این احتمال وجود دارد که از اوایل سن بلوغ به سمعک نیاز داشته باشند. به طور معمول سمعک در افرادی که ناشنوایی ناشی از سندرم آلپورت دارند، بسیار مفید است.
شروع، پیشرفت و شدت کاهش شنوایی در سندرم آلپورت به دلیل بخشی ژنتیکی خاص که در هر فرد وجود دارد، بسیار متفاوت است. کاهش شنوایی در زنان مبتلا به XLAS کمتر از مردان اتفاق میافتد و به طور معمول در اواخر زندگی آنها رخ میدهد، اگرچه درصد کمتری از زنان در سن نوجوانی دچار کاهش شنوایی میشوند. به طور معمول مردان و زنان مبتلا به ARAS در اواخر کودکی یا اوایل نوجوانی دچار کم شنوایی میشوند. این احتمال وجود دارد که در افراد مبتلا به ADAS کم شنوایی ایجاد شود، اگرچه این اتفاق خیلی دیرتر و به طور معمول در افراد مسن رخ میدهد.
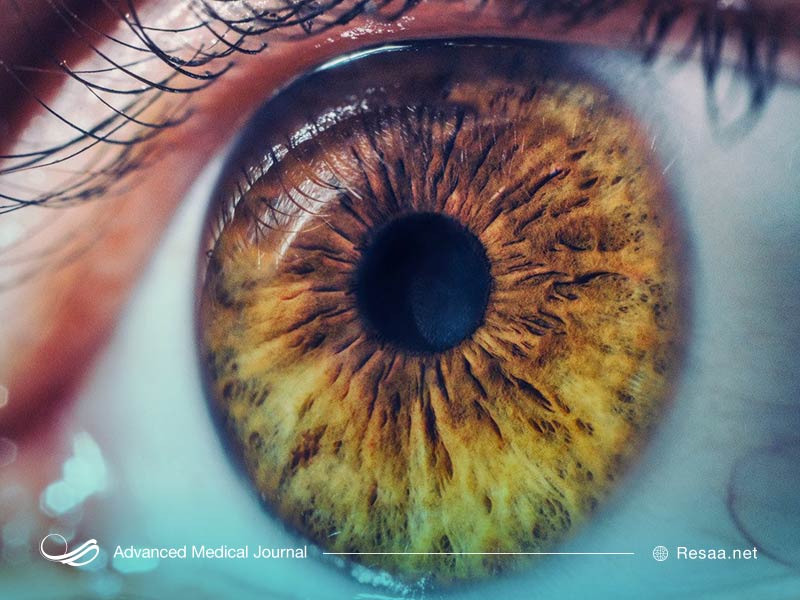
افراد مبتلا به سندرم آلپورت نیز ممکن است در چندین بخش از چشم از جمله عدسی، شبکیه و قرنیه دچار ناهنجاری شوند. ناهنجاریهای چشمی ناشی از XLAS و ARAS در ارائه و بروز عوارض بسیار مشابه هستند. ناهنجاریهای چشم در ADAS غیر معمول یا غیررایج است.
قدامی لنتیکونوس “lenticonus” وضعیتی است که در آن لنزهای چشم به طور غیرطبیعی شکل میگیرند، به طور خاص عدسی به جلو و در فضای (اتاق قدامی) پشت قرنیه برجسته میشود. لنتیکونوس قدامی میتواند باعث عینکی شدن فرد بیمار شود و گاهی منجر به تشکیل آب مروارید میگردد. قدامی لنتیکونوس در حدود 20٪ از مردان مبتلا به XLAS رخ میدهد و اغلب در اواخر بلوغ یا اوایل بزرگسالی مشخص میشود.
شبکیه، غشای حساس به نور و غنی از اعصاب است که پشت چشم را میپوشاند، همچنین این احتمال وجود دارد که تحت تأثیر تغییرات رنگی ایجاد شده و در اثر ایجاد ترکهای زرد یا سفید به صورت سطحی در شبکیه قرار گیرد. به نظر نمیرسد که این تغییرات بینایی را تحت تأثیر قرار دهند. بیماران نادر دچار نازک شدن تدریجی شبکیه میشوند که این وضعیت ممکن است منجر به ایجاد سوراخهایی (سوراخهای ماکولار “macular”) شود که میتواند بینایی را مختل کند.
این احتمال وجود دارد که قرنیه که لایه بیرونی شفاف (transparent) چشم است نیز تحت تأثیر قرار گیرد؛ اگرچه ناهنجاریهای خاص ممکن است متفاوت باشند. اثرات روی قرنیه ممکن است به آرامی و پیشرونده باشند. فرسایشهای مکرر قرنیه که در آن لایه خارجی قرنیه (اپیتلیوم “epithelium”) به چشم نمیچسبد، ممکن است به آرامی رخ دهد. فرسایش مکرر قرنیه میتواند باعث ناراحتی یا درد شدید چشم، حساسیت غیرطبیعی به نور (فوتوفوبیا ” photophobia”)، تاری دید و احساس وجود جسم خارجی (مانند کثیفی یا مژه) در چشم شود. دیستروفی چند شکلی قرنیه خلفی نیز ممکن است رخ دهد. این احتمال وجود دارد که اثرات روی قرنیه به آرامی پیشرونده باشد. هر دو چشم ممکن است تحت تأثیر قرار بگیرند. یک چشم می تواند بیش از چشم دیگر تحت تأثیر قرار گیرد. در موارد شدید، دیستروفی چند شکلی قرنیه خلفی میتواند باعث تورم (ادم) یک لایه خاص از قرنیه، فوتوفوبیا، احساس جسم خارجی (مانند خاک یا مژه) در چشم و کاهش بینایی شود.
علائم اضافی می توانند در افراد خاص مبتلا به سندرم آلپورت رخ دهد. در تعداد کمی از مردان، آنوریسمهای قفسه سینه یا قسمتهای شکمی آئورت، شریان اصلی که خون را از قلب دور میکند، رخ داده است. آنوریسم زمانی اتفاق میافتد که دیواره رگهای خونی به صورت بالون در آمده یا به سمت بیرون برآید، به طور بالقوه پاره شود و باعث خونریزی در بدن گردد.
علل بروز و ابتلا به سندرم آلپورت چیست؟
سندرم آلپورت توسط انواع وضعیتهای بیماریزا در توالی DNA ژنهای خاص ایجاد میشود. ژنها دستورالعملهایی را برای ایجاد پروتئینهایی ارائه میدهند که نقشی اساسی در بسیاری از عملکردهای بدن دارند. هنگامی که یک نوع عامل بیماریزا در توالی DNA ژنهای یک ژن رخ میدهد، این احتمال وجود دارد که محصول پروتئین معیوب، ناکارآمد یا فاقد آن باشد. بسته به عملکرد پروتئین خاص، این وضعیت میتواند بر بسیاری از سیستمهای اندام بدن تأثیر بگذارد.
ژن COL4A5 در کروموزوم X قرار دارد. ژنهای COL4A3 و COL4A4 روی کروموزوم 2 قرار دارند. کروموزومها که در هسته سلولهای انسان وجود دارند، اطلاعات ژنتیکی هر فرد را حمل میکنند. سلولهای بدن انسان به طور معمول 46 کروموزوم دارند. جفتهای کروموزومهای انسانی از 1 تا 22 شمارهگذاری شده و کروموزومهای جنسی X و Y مشخص میشوند. مردان دارای یک کروموزوم X و یک Y و زنان دو کروموزوم X هستند.
سندرم آلپورت مرتبط با X ناشی از انواع بیماریزا در ژن COL4A5 است که در کروموزوم X قرار دارد. اختلالات مرتبط با X در مردان مبتلا علائم شدیدتری نسبت به زنان مبتلا ایجاد میکند. زنان دو کروموزوم X در سلولهای خود دارند اما یکی از کروموزومهای X در حین رشد “خاموش” یا غیرفعال میشود، فرایندی که “لیونیزاسیون” نامیده میشود و تمام ژنهای آن کروموزوم غیرفعال میشوند. لیونیزاسیون یک فرآیند تصادفی است و از بافتی به بافت دیگر متفاوت است. این شرایط در بافتها نیز میتواند از سلولی به سلول دیگر متفاوت باشد. زنانی که دارای ژن بیماری در یک کروموزوم X هستند، برای آن اختلال هتروزیگوت هستند؛ به این معنی است که یک نسخه غیر طبیعی از ژن و یک نسخه طبیعی دارند. در نتیجه فرآیند لیونیزاسیون، اکثر زنان هتروزیگوت حدود 50٪ X طبیعی و 50٪ جهش X بیان شده در هر بافت را دارند و به طور معمول فقط علائم خفیفتر این اختلال را نشان میدهند.
به دلیل تصادفی بودن روند لیونیزاسیون، موارد استثنایی در این قاعده وجود دارد، به ویژه اگر غیرفعال شدن یک نسخه از کروموزوم X به نفع یکی از نسخهها به طور قابل توجهی “در جهت متفاوت” باشد. اگر نسخه طبیعی غالب شود، زنان هتروزیگوت میتوانند کاملا بدون علامت باشند و در شرایط معمول و نرمال قرار بگیرند. اگر نسخه جهش یافته غالب باشد، زنان هتروزیگوت میتوانند به شدت مانند مردان تحت تأثیر قرار گیرند.
جمعیتهای تحت تأثیر سندرم آلپورت
تخمین زده میشود که سندرم آلپورت تقریباً از هر 5،000 تا 10،000 نفر جمعیت عمومی در ایالات متحده، یک نفر را درگیر کند، به این معنی که تقریباً 30،000 – 60،000 نفر در ایالات متحده این اختلال را دارند. سندرم آلپورت 3 درصد از کودکان مبتلا به بیماری مزمن کلیه و 0.2 درصد از بزرگسالان مبتلا به بیماری کلیه در مرحله نهایی را در ایالات متحده شامل میشود. در XLAS، مردان بیش از زنان تحت تأثیر قرار میگیرند. در اشکال اتوزومال سندرم آلپورت، مردان و زنان با شدت برابر تحت تأثیر قرار میگیرند.
اختلالات مرتبط به سندرم آلپورت
علائم اختلالات زیر میتواند شبیه علائم سندرم آلپورت باشند. مقایسه ممکن است به منظور تشخیص افتراقی مفید باشد.
- افراد نادر مبتلا به سندرم آلپورت مرتبط با X دارای نقص ژنتیکی خاصی هستند که به عنوان سندرم ژن مجاور شناخته میشود و میتوانند به لیومیوماتوز مبتلا شوند، این بیماری با رشد (تکثیر) کنترل نشده سلولهای عضله صاف مشخص میشود. زنان مبتلا غالباً دچار ضخیم شدن پوست مجرا و کلیتوریس (هیپرتروفی ولو و کلیتورال) میشوند. در افراد مبتلا به این اختلال علائم سندرم آلپورت از جمله بیماری پیشرونده کلیه و کاهش شنوایی نیز مشاهده میشود.
- کمپلکس AMME یک بیماری بسیار نادر است که فقط در تعداد معدودی از افراد در چند خانواده (اقوام) توصیف شده است. AMME مخفف سندرم آلپورت، ناتوانی ذهنی، هیپوپلازی میان سطح و بیضوی است.
- نفروپاتی غشای زیرین نازک (TBMN) اصطلاحی است که اغلب به منظور توصیف افرادی که هماچوری بدون سایر علائم بیماری کلیه دارند، غشاهای پایه نازک گلومرولی (GBM) در بیوپسی کلیه و سابقه خانوادگی منفی برای نارسایی کلیه استفاده میشود. میزان زیادی از همپوشانی بین سندرم آلپورت و به اصطلاح TBMN وجود دارد.
- بسیاری از اختلالات وجود دارند که در آن هماچوری مداوم یک علامت برجسته است. این اختلالات شامل نفروپاتی IgA، بیماری رسوب متراکم، کم خونی سلول داسی شکل، بیماری کلیه کیستیک، سندرم اورمیک همولیتیک غیرمعمول و نفروپاتی C3 است. سایر اشکال خانوادگی بیماری پیشرونده کلیه شامل بیماری کلیه پلی کیستیک، نفروونوفیز و بیماری فابری است. تعدادی از اختلالات ژنتیکی نادر وجود دارند که در آنها بیماری کلیوی با کاهش شنوایی همراه است.
روشهای درمانی استاندارد سندرم آلپورت
درمان سندرم آلپورت به سمت علائم خاصی است که در هر فرد مشخص است. درمان ممکن است به تلاش هماهنگ تیمی از متخصصان نیاز داشته باشد. متخصصان اطفال، نفرولوژیستها، شنوایی سنجیها، چشم پزشکان و سایر متخصصان مراقبتهای بهداشتی ممکن است نیاز به برنامهریزی منظم و همه جانبه برای تأثیرگذاری در درمان کودک داشته باشند. مشاوره ژنتیک برای افراد مبتلا و خانوادههای آنها توصیه میشود. حمایت روانی-اجتماعی از کل خانواده نیز ضروری است.
از داروهایی که به عنوان مهار کنندههای آنزیم مبدل آنژیوتانسین (ACE) شناخته میشوند، برای درمان افراد مبتلا به سندرم آلپورت استفاده شده است. دادههای تاریخی پزشکی نشان میدهد که درمان زودهنگام با مهار کنندههای ACE میتواند پیشرفت در مرحله نهایی بیماری کلیوی را در مردان و زنان مبتلا به سندرم آلپورت به تأخیر بیندازد.


سلام من بیماری سندرم آلپورت دارم آیا برای مشکل شنوایی به جزسمعک راه حل دیگه ای وجود دارد مثلا استفاده ازدارو یاعمل جراحی گوش
توسط مهدی در 30 دسامبر 2021با سلام و وقت بخیر. در حال حاضر درمان دیگری برای کمک به شنوایی یا برگشت آن وجود ندارد ولی تحقیقات برای درمانهای احتمالی دیگر در حال انجام است.
توسط دکتر مریم تجریشی در 9 ژانویه 2022